상 전이phase transition는 두 상이 서로 화학 퍼텐셜chemical potential이 달라서 나타는 현상이다. 두 상 α와 β가 평형을 이루고 있다면 두 상의 화학 퍼텐셜이 같다는 것이다. 이를 식으로 표현하면 아래와 같다.
μα(p,T)=μβ(p,T)
(1)
상과 상의 경계선의 기울기는 압력p와 온도T를 가지고 논의하는 것이 가장 편리하다. 두 상이 평형을 이루고 있는 계에 압력을 가하면 평형이 깨진다. 이 계는 그에 대응하여 온도가 변하면서 평형이 회복되고, 두 상이 평형을 이루는 압력p과 온도T가 변하게 된다. 즉, 압력이나 온도를 바꿀 때 평형을 유지시켜주는 dp와 dT 사이에 관계가 존재한다.

평형 상태에 있는 두 상에서 p와 T를 미소하게 변화시키는 과정에도 두 상 사이의 평형상태가 계속해서 유지되고 있다면,
dμα(p,T)d=μβ(p,T)
(2)
식(2)는 동적인 평형이기 때문에 등호가 성립된다. 또 한편, dG=Vdp - SdT라고 쓸 수 있으므로, 화학 퍼텐셜μ은 몰 깁스 에너지이므로 dμ=-SmdT+Vmdp로 쓸 수 있다. 식(2)를 바꿔쓰면,
(3)
이를 dp와 dT에 대해서 정리하면,
(4)
식(4)를 dp/dT로 표현하면 아래와 같다.
(5)
이 식(5)를 Clapeyron 식,Clapeyron equation이라고 한다.
고체-액체의 상 경계
고체가 액체로 녹는 용융 과정에서는 몰 엔탈피 변화ΔtrsH가 수반된다. 온도 T에서 변화가 이루어질 때, ΔfusS=ΔfusH/T 이므로, Clapeyron 식을 다음과 같이 쓸 수 있다.
(6)
일반적으로 용융 과정에서의 몰 엔탈피 변화는 ΔfusH>0 이고, ΔfusV>0 이므로 고체-액체의 상 경계의 기울기는 dp/dT>0 이다. 또 ΔfusH와 ΔfusV는 온도와 압력에 무관하고, 압력이 p*일 때 녹는점이 T*, p 일때 T 라고 하면 식(6)의을 적분형태로 바꾸면
(7)
식(7)을 적분하면,
(8)
ln(1+x)를 Taylor 전개를 하면,
(9)
그리고 x<<1 이라면 ln(1+x)≒x 이다. 따라서 식(8)의 lnT/T*는 아래처럼 쓸 수 있다.
(10)
그래서 T가 T*에 가까운 경우에는 식(10)을 식(8)에 대입하여 쓸 수 있다.

(11)
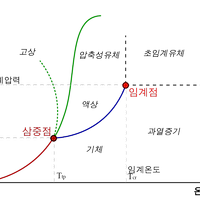
즉 p와 T에 대한 1차함수가 나온다. 고체상과 액체상의 경계를 보면 1차함수와 같은 직선으로 이루어져 있음을 확인할 수 있다.
액체-기체의 상 경계
(12)
식(12)에서 일반적으로 기체의 몰부피가 액체의 몰부피보다 훨씬 크므로 즉, Vm(g)>>Vm(l) 이므로, ΔvapV ≒ Vm(g)로 볼 수 있다. 또 기체가 이상기체라고 가정하면 Vm(g)=RT/p 가 되므로 식(12)는 아래처럼 다시 쓸 수 있다.
(13)
여기서 dx(1/x)=d(lnx)의 수학적 관계를 이용하면 식(13)은 아래처럼 다시 쓸 수 있다.
(14)
식(14)를 Cuausius-Clapeyron 식, Cuausius-Clapeyron Equation이라고 한다. 식(14)를 또 ΔvapH가 온도와 압력에 무관하고,T*에서의 증기압이 p*이고 T에서의 증기압이 p라고 하고 적분형태로 고치면,
(15)
이를 적분하면,
(16)

좌변의 ln항을 없애서 지수함수 형태로 고치면,
(17)
즉, 지수함수형태의 꼴이 된다. 그래서 오른쪽의 그림처럼 액체상과 기체상의 경계는 지수함수 형태임을 확인할 수 있다.
고체-기체의 상 경계
액체-기체 상경계식인 식(17)에서 ΔvapH가 ΔsubH로 바뀐다. ΔsubH는 ΔvapH와 ΔfusH의 합으로 주어진다. 따라서 고체-기체의 상 경계식은

(18)
역시 지수함수의 형태로 주어진다.
'Physical Chemistry > Thermodynamics' 카테고리의 다른 글
| 상의 안정도와 상 전이, Phase Transition (1) | 2014.11.05 |
|---|---|
| 순수한 물질의 상 (0) | 2014.08.12 |
| Gibbs 에너지의 성질 (1) | 2014.08.09 |
| 1법칙과 2법칙의 결합, Combining the First and Second Laws (0) | 2014.08.08 |
| 자발성에 대한 기준, Criteria for Spontaneity (4) | 2014.05.03 |