실험 목적 - 분광 광도계를 이용하여 미지 농도의 황산구리 용액의 농도를 결정한다.
- 황산구리
구리의 황산염. 1가의 황산구리(I) 및 2가의 황산구리(II)가 알려져있다.
황산구리(I) (황산 제일구리) : 화학식은
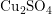
로, 무색 또는 회색의 분말이다. 물 속에 넣거나 습한 공기 속에 방치하면 황산구리(II)가 된다. 200℃로 가열한 진한 황산에 구리를 녹여, 알코올로 처리하면 얻을 수 있다.
황산구리(II) (황산 제이구리) : 화학식은
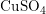
이며 청색의 투명한 결정으로 비중은 2.286 이다. 건조한 공기 중에 두면 서서히 수분을 잃고 가루가 된다. 가열하면 45℃에서 2분자의 물, 110℃에서 4분자의 물, 다시 250℃에서 모든 물분자를 잃고 무색의 무수물이 된다. 황산구리(II)에 수산화나트륨을 넣고 가열하면 염기성 산화구리가 되어 흑색으로 바뀐다.
무수물로 존재하기도 하고 5수화물(
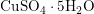
)로 존재하기도 하는데, 무수물은 물분자가 모두 빠져나간 상태의 분자를 말하며, 5수화물은 분자주변에 물분자가 5개 붙어있는 상태를 말한다. 무수물은 백색의 분말로 비중 비중 3.03, 100g의 물에 0℃에서 14.3g, 100℃에서 75.4g 녹는다. 메탄올에는 조금 녹지만 에탄올에는 녹지 않는다. 5수화물은 구리에 묽은 황산과 공기를 반응시키거나, 산화구리를 묽은 황산에 녹인 후 증발과 농축의 과정을 거쳐 결정화하면 얻어진다.
- 분광 광도법
분광광도법은 화학 농도의 측정에 전자기 복사선을 이용하는 방법이다. 화합물을 분광광도법으로 분석하기 위해서는 화합물이 전자기 복사선을 흡수해야 할 뿐만 아니라, 이들의 흡수는 시료 중에 있는 다른 화학종에 의한 흡수로부터 구별될 수 있어야한다. 대부분의 화합물들이 자외복사선을 흡수할 때는 그 결과가 정확하지 못한 경향이 있으므로, 분석은 주로 가시 스펙트럼으로 제한한다. 만약 시료중에 방해 화학종이 없다면, 자외선 흡광도도 이용할 수 있다. 생화학자들은 주로 자외선 영역인 280nm에서 단백질을 분석한다. 그 이유는 실제적으로 모든 단백질에 존재하는 방향족 고리가 280nm에서 최대 흡광도를 나타내기 때문이다. 염, 완충용액 및 탄수화물 등과 같은 그 밖의 일반적인 용질들은 이 파장에서 흡광도를 거의 또는 전혀 나타내지 않는다.
- 투광도와 흡광도
분자가 광자를 흡수하면 분자의 에너지는 증가된다. 이 때 분자는 들 뜬 상태로 올라갔다고 말한다. 만약 분자가 광자를 방출하게 되면, 그 분자의 에너지는 낮아진다. 최저 에너지 상태를 바닥상태라고 한다.
시료에 의해서 빛이 흡수되면 빛살(beam of light)의 복사세기(radiant power)는 감소한다. 복사세기,
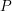
는 빛살의 단위면적당, 단위시간당 에너지를 의미한다. 분광광도법의 모형을 아래 그림에 표시했다.

[그림1. 분광광도법 실험의 모형도]
빛은 단일 파장이 얻어지도록 단색화장치(monochromator : 프리즘, 회전발 또는 필터)를 통과한다. 단색화된 빛은 한 가지 파장만을 갖는 빛이다. 길이
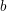
인 시료에 복사세기가
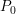
인 단색파장의 빛을 쪼여준다. 쪼여주는 반대편 쪽으로 시료를 통과하여 나온 빛살의 복사세기는
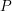
이다. 빛의 일부는 시료에 의해서 흡수될 것이므로,
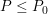
이다.
투광도(transmittance),
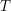
는 원래의 쪼여준 빛과 시료를 통과한 빛의 분율로서 정의된다.
그러므로
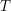
는 0에서 1사이의 범위를 가진다. 퍼센트 투광도(percent transmittance)는 단순히
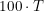
로서, 0과 100% 사이의 범위를 가진다. 이보다 더 유용한 양은 흡광도(Absorbance,
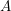
)로서, 때로는 광도(optical density)라고도 한다. 흡광도는 다음과 같다.
전혀 빛이 흡수되지 않았을 때는
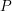
=
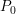
이며,
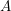
=0 이다. 만약 90%의 빛이 흡수되었다면, 10%가 투과되었으므로
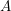
=1이 된다. 그리고 1%의 빛만이 투과되었다면
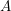
=2가 된다. 흡광도가 중요한 이유는 이것이 시료중에 포함되어 있는 빛을 흡수하는 화학종의 농도에 정비례하기 때문이다.
- Beer-Lambert 법칙
흡광도
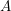
는 단위가 없다. 하지만 어떤 책의 저자들은 흡광도 다음에 '흡광도 단위'를 나타낸다. 시료의 농도,

는 주로 리터당 몰의 단위(
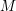
)로 나타내고, 빛이 통과하는 길이
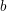
는 보통 센티미터로 표시한다.

는 몰 흡광계수로,
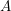
의 단위가 없기 때문에

의 단위는
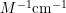
이다. 몰 흡광계수는 특정 파장의 빛을 얼마만큼 흡수하였는가를 나타내는 물질의 특성이다.
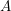
와

값은 빛의 파장에 의존하기 때문에 Beer-Lambert 법칙은 다음과 같이 나타낼 수 있다.

는 흡광도와
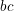
곱 사이의 단순한 비례상수이다.

값이 클 수록
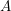
는 커진다.


